
Informazioni sull'autore
Mohammed Giobbe
Regulatory Consultant (Pharmacist BSc, Biomedical Informatics MSc). Con 19 anni di esperienza lavorativa presso SFDA, aziende multinazionali e come consulente professionista.
L’Autorità saudita per gli alimenti e i farmaci ( SFDA ) richiede ai produttori di dispositivi medici di nominare un rappresentante autorizzato (AR) in Arabia Saudita prima di commercializzare i loro prodotti. L’AR sarà il rappresentante locale responsabile delle attività normative come la registrazione dei dispositivi medici e la sorveglianza post-marketing.
La nomina di un rappresentante autorizzato richiede la presentazione di un accordo firmato alla SFDA . Si tratta di una procedura rapida e il produttore può modificare il rappresentante autorizzato in modo analogo. Ecco alcune note iniziali:
- La nomina di un AR è un processo che dura da 1 a 2 settimane.
- È possibile modificare l’AR in qualsiasi momento.
- I produttori possono nominare più AR (a determinate condizioni).
- Prima di registrare e commercializzare il dispositivo è necessaria una licenza AR valida.
- Per poter autorizzare la spedizione è necessaria una licenza AR valida.
In questo post analizzeremo il ruolo della realtà aumentata e come nominarne uno per la tua azienda.
Sommario
Che cosa è un rappresentante autorizzato?
Il rappresentante autorizzato è la società saudita locale che rappresenta legalmente il produttore internazionale di dispositivi medici in Arabia Saudita. SFDA richiede alle aziende di nominare un rappresentante autorizzato prima di registrare il proprio prodotto; il rappresentante autorizzato non è necessariamente il distributore.
AR indipendente vs distributore come AR
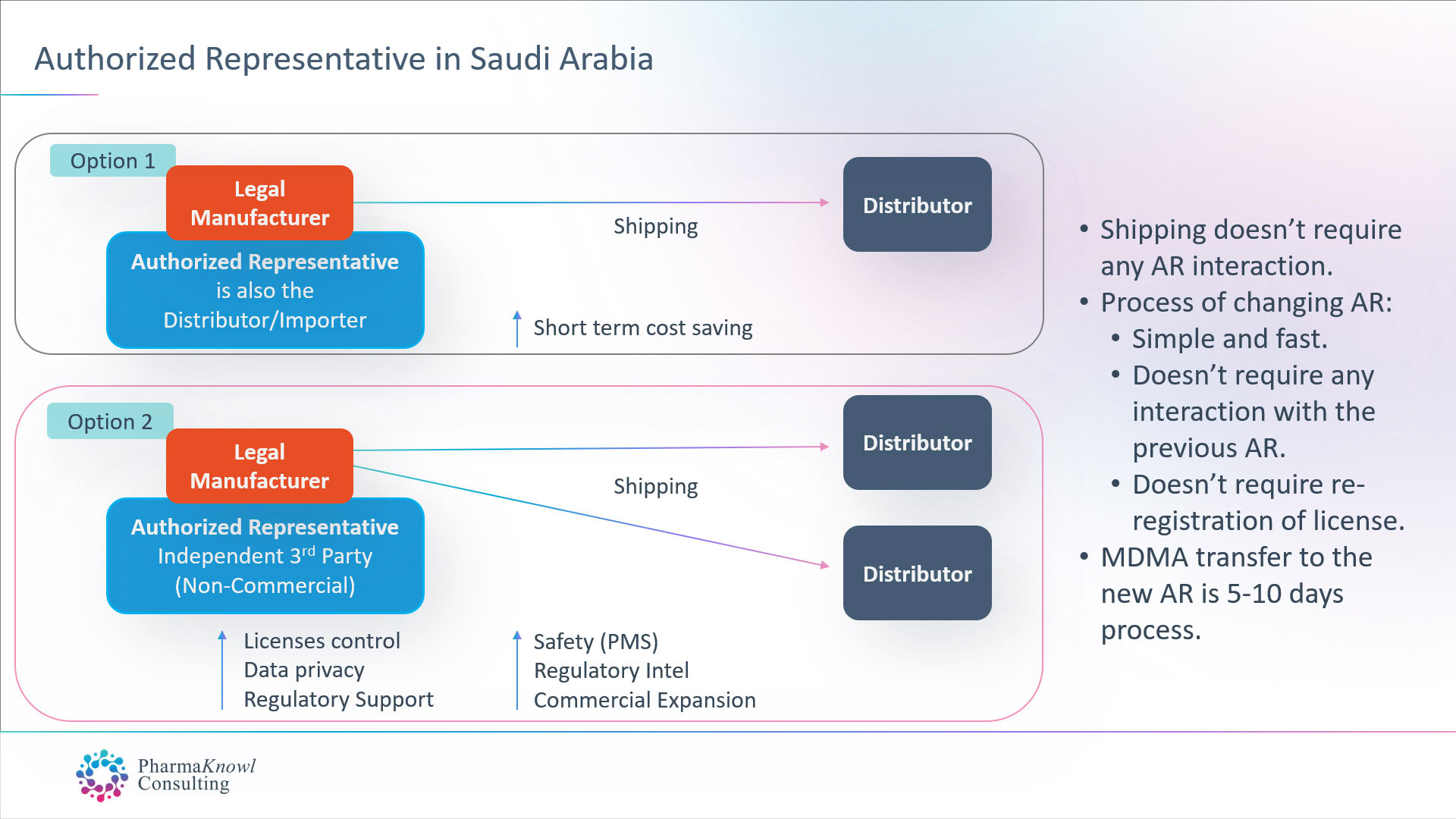
I produttori internazionali di dispositivi medici hanno due opzioni quando vogliono nominare un AR in Arabia Saudita:
- Nominare il proprio distributore commerciale come proprio AR.
- Nominare un AR indipendente (non commerciale).
La maggior parte dei produttori legali preferisce nominare un AR indipendente poiché è la migliore opzione in Arabia Saudita, simile alla prassi comune nell’UE.
Vantaggi della realtà aumentata indipendente
Il pagamento di una quota fissa annuale per un AR indipendente senza alcuna commissione sulle spedizioni offre ai produttori una serie di vantaggi, quali:
- Supporto normativo e post-marketing avanzato.
- Possibilità di registrare più marchi per lo stesso prodotto.
- Possibilità di spedire merci a più distributori/importatori.
- Operazioni aziendali stabili.
- Controllo sulle licenze dei prodotti
- Riservatezza dei dati.
- Consigli imparziali e approfondimenti di mercato.
- Informazioni normative puntuali.
- Ottime capacità comunicative.
Responsabilità
L’AR deve fornire quanto segue al produttore legale:
- Rappresentanza legale autorizzata presso SFDA
- Supporto normativo
- Invia l’identificazione univoca del dispositivo ( SFDA UDI )
- Chiarimenti sulle normative SFDA
- Informazioni e approfondimenti di mercato
- Aggiornamenti MDMA
- Sorveglianza post-marketing
- Segnalazione di eventi avversi e incidenze
- Presentazione delle azioni correttive
- Condurre un follow-up clinico post-marketing (PMCF) in Arabia Saudita
- Facilitare la manutenzione del dispositivo
- Supporto per problemi di sdoganamento delle spedizioni
Qualità standard AR
- Ottima copertura dei compiti essenziali
Conformità alle normative, monitoraggio della sicurezza, capacità di comunicazione, ecc. - Intelligence normativa:
Condividere tempestivamente gli aggiornamenti normativi con la possibilità di identificare le aree di impatto e i livelli di rischio. - Buon accesso a SFDA
Per supporto e risoluzione dei problemi. - Capacità di pianificazione della supply chain
Ad esempio per gli orari di arrivo rispetto alle date di approvazione e ai permessi di importazione - Lavorare sui sistemi elettronici del produttore
Per aggiornare le scadenze normative quali date di registrazione, scadenze, rinnovi, ecc. - Supportare le ispezioni SFDA
- Facilita le pratiche di spedizione al porto.
- Risolvere altri problemi presenti sul mercato.

Classi a basso rischio
In passato, SFDA richiedeva l’AR solo per le classi ad alto rischio. Tuttavia, dal 27 settembre 2022, l’AR è diventata obbligatoria anche per i dispositivi a basso rischio. Ciò ha coinciso con l’ annullamento della procedura di registrazione per i dispositivi a basso rischio (MDNR).
Requisiti della licenza
Di seguito elenchiamo i requisiti SFDA affinché un’azienda locale possa agire come rappresentante autorizzato:
- Un’azienda saudita con un record commerciale (CR) di attività nel settore dei dispositivi medici.
- Disponibilità di un sistema di gestione della qualità (QMS)
- Un certificato ISO 13485 valido.
- Superare l’ispezione SFDA
- Una licenza valida per l’esercizio di dispositivi medici SFDA (MDEL)
- Personale dedicato alle funzioni di sicurezza e regolamentazione.
- Contratto di rappresentanza autorizzata firmato con il produttore legale.
Accordo AR
La SFDA impone uno specifico modello di accordo AR che deve essere firmato così come avviene tra i produttori legali e il loro rappresentante autorizzato saudita.
Ecco alcune note essenziali correlate:
- I produttori possono nominare più AR (a determinate condizioni).
- L’accordo AR deve essere apostillato o legalizzato.
- La validità minima dell’AR è di un anno.
- La validità dell’AR corrisponde alla durata dell’accordo o è più breve.
Modifica del rappresentante autorizzato
La modifica del rappresentante autorizzato in Arabia Saudita non richiede l’approvazione del precedente AR. La procedura richiede una settimana, seguita dal trasferimento delle licenze per dispositivi medici (MDMA). Pertanto, non è necessario registrare nuovamente i prodotti dopo il trasferimento dell’AR.
Commissioni
La tassa di licenza SFDA per un certificato di rappresentante autorizzato è di 2.600 SAR all’anno (693,33 USD). Per maggiori dettagli sulle tariffe SFDA , consulta il nostro articolo: Tariffe SFDA .
Fornitore rappresentante autorizzato
PharmaKnowl è un rappresentante autorizzato con licenza SFDA , di cui si fidano famose aziende di dispositivi medici e MedTech in tutto il mondo. Se avete bisogno di un rappresentante autorizzato per il vostro primo ingresso sul mercato o per trasferirvi da un rappresentante autorizzato già esistente in Arabia Saudita, contattateci per ricevere una proposta. Potete anche fissare un incontro con noi per rispondere alle vostre domande.
Per saperne di più
Registrazione SFDA



