
关于作者
穆罕默德·喬布蘭
監管顧問(藥劑師理學學士、生物醫學資訊學碩士)。擁有 19 年的 SFDA 和跨國公司工作經驗,並擔任專業顧問。
沙特食品药品管理局 (SFDA 要求医疗器械制造商在销售其商品之前,必须在沙特阿拉伯指定一名授权代表 (AR)。AR 将是负责 医疗器械注册 和上市后监测等监管活动的当地代表。
指定授权代表需要向 SFDA 提交已签署的协议。这是一个快速的过程,制造商可以类似 地更换授权代表 。以下是一些初步说明:
- 任命 AR 是一个 1-2 周的过程。
- 可以随时更改 AR。
- 制造商可以指定多个 AR(有条件)。
- 在设备注册和营销之前,需要有效的 AR 许可证。
- 货件清关需要有效的 AR 许可证。
这篇文章将讨论 AR 角色以及如何为您的公司指定一个。
什么是授权代表?
授权代表是合法代表沙特阿拉伯国际医疗器械制造商的沙特当地公司。 SFDA 要求公司在注册其产品之前指定 AR;AR 不一定是分销商。
作为 AR 的独立 AR 与分销商
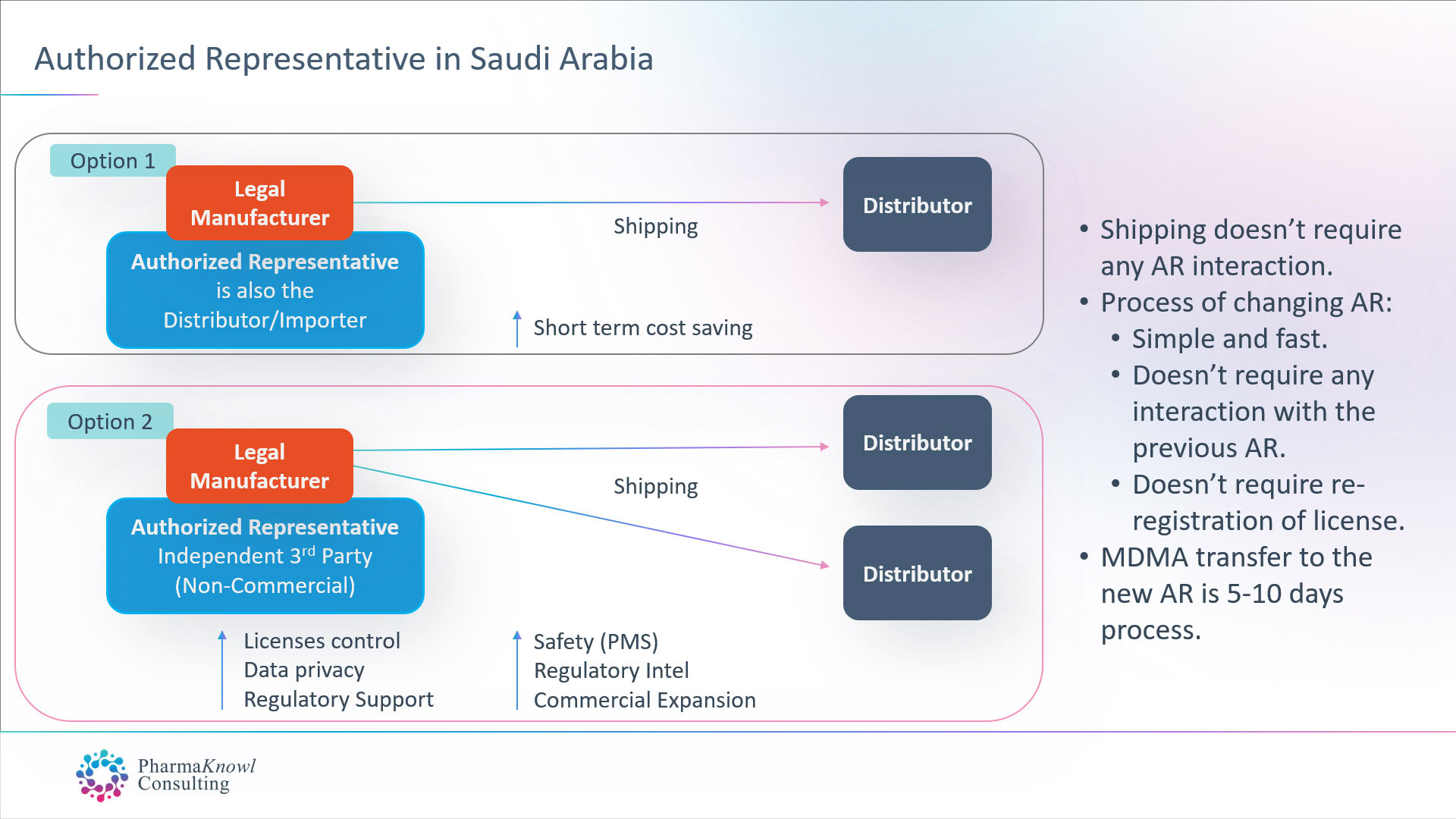
当国际医疗器械制造商想在沙特指定 AR 时,他们有两种选择:
- 指定他们的商业分销商作为他们的 AR。
- 指定独立的 AR(非商业性)。
大多数合法制造商更喜欢指定独立的 AR,因为这是沙特的最佳选择,类似于欧盟的普遍做法。
独立 AR 优势
为独立的 AR 支付年度固定费用,无需任何货运佣金,为制造商提供了一系列优势,例如:
- 高级监管和上市后支持。
- 能够为同一商品注册多个品牌名称。
- 能够将货物运送给多个分销商/进口商。
- 稳定的业务运营。
- 控制产品许可证
- 数据机密性。
- 公正的建议和市场洞察。
- 及时的监管情报。
- 高沟通能力。
责任
AR 必须向合法制造商提供以下内容:
- SFDA 的合法授权代表
- 法规支持
- 提交唯一设备标识 (SFDA UDI)
- SFDA 法规澄清SFDA
- 市场情报和洞察
- MDMA 更新
- 上市后监测
- 报告不良事件和发生率
- 提交纠正措施
- 在沙特阿拉伯进行上市后临床随访 (PMCF)
- 便于设备维护
- 支持货件清关问题
AR 标准质量
- 出色地覆盖基本职责
法规遵从性、安全监控、沟通技巧等 - 监管情报:
及时共享监管更新,并能够识别影响区域和风险级别。 - 交通便利 SFDA
用于支持和解决问题。 - 供应链规划功能
例如,到达时间表与批准日期和进口许可证 - 在制造商 e-systems 上工作
更新监管里程碑,例如注册日期、到期、续订等。 - 支持 SFDA 检查
- 方便在港口办理货物手续。
- 解决其他市场内问题。

低风险等级
过去, SFDA 过去只要求高风险类别进行 AR。但是,自 2022 年 9 月 27 日起,AR 也已成为低风险设备的强制性要求。它恰逢低风险注册程序 (MDNR) 的取消 。
许可证要求
在这里,我们列出了 SFDA 对本地公司担任授权代表的要求:
- 一家拥有医疗器械活动商业记录 (CR) 的沙特公司。
- 质量管理体系 (QMS) 的可用性
- 有效的 ISO 13485 证书。
- 通过 SFDA 检查
- 有效的 SFDA 医疗器械企业许可证 (MDEL)
- 负责安全和监管职能的专职人员。
- 与合法制造商签署授权代表协议。
AR 协议
SFDA 规定了特定的 AR 协议模板,该协议模板需要在合法制造商与其沙特授权代表之间签署。
以下是一些重要的相关说明:
- 制造商可以指定多个 AR(有条件)。
- AR 协议必须经过海牙认证或合法化。
- AR 的最短有效期为一年。
- AR 有效期与协议持续时间匹配或更短。
更改您的授权代表
更改沙特的授权代表不需要前任 AR 的批准。该过程需要一周时间,然后是医疗器械许可证 (MDMA) 的转移。因此,转让 AR 后无需重新注册产品。
费用
授权代表证书的 SFDA 许可费用为 2,600 沙特里亚尔/年(693.33 美元)。有关 SFDA 费用的更多详细信息,请参阅我们的文章: SFDA 费用。
授权代表提供商
PharmaKnowl 是 SFDA 许可的授权代表,受到全球著名医疗器械和医疗技术公司的信赖。如果您需要 AR 作为您的首次市场进入或从沙特阿拉伯的现有 AR 转移,请联系我们以获取提案。您还可以安排与我们会面以回答您的问题。
阅读更多
SFDA 注册



