
عن الكاتب
محرر التنظيمات
نشر من قبل قسم الشؤون التنظيمية في فارمانول للإستشارات، الرياض.
تشترط الهيئة السعودية للغذاء والدواء على جميع شركات الأجهزة الطبية في المملكة العربية السعودية الالتزام بقواعد التعريف الفريد للأجهزة (UDI). ويتعين على هذه الشركات تسجيل معلومات التعريف الفريد للأجهزة الخاصة بمنتجاتها في نظام التعريف الفريد للأجهزة (UDI) التابع للهيئة. ويتم تطبيق القواعد تدريجيًا بناءً على فئة مخاطر الجهاز ولا يمكن تقديمها إلا من خلال الممثل المعتمد في المملكة العربية السعودية.
ما هو UDI؟
معرف الجهاز الفريد (UDI) عبارة عن سلسلة من الأحرف الرقمية أو الأبجدية الرقمية التي يتم إنشاؤها من خلال نظام ترميز مقبول عالميًا. وهو معرف يحدد الجهاز بشكل لا لبس فيه من خلال توزيعه واستخدامه. يتكون من جزأين:
1. معرف الجهاز (DI): جزء ثابت إلزامي من معرف الجهاز (UDI) الذي يحدد رقم المنتج المحدد للجهاز وصانع الملصق الخاص بهذا الجهاز و
2. معرف الإنتاج (PI): جزء متغير مشروط من معرف الإنتاج الفريد (UDI) يحدد واحدًا أو أكثر من العناصر التالية عند تضمينها على ملصق الجهاز:
- الدفعة أو المجموعة التي تم تصنيع الجهاز ضمنها.
- الرقم التسلسلي لجهاز معين.
- تاريخ انتهاء صلاحية جهاز معين.
- تاريخ تصنيع جهاز معين.
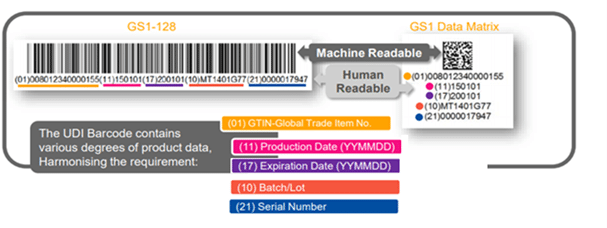
يجب وضع معرف المنتج الفريد (UDI) على ملصق الجهاز والمستويات الأعلى من مواد التغليف وتقديمه في شكلين:
- نص عادي سهل القراءة (يُعرف أيضًا باسم التفسير القابل للقراءة من قبل الإنسان HRI)، و
- تكنولوجيا AIDC (التعرف التلقائي والتقاط البيانات).
رمز UDI الشريطي – ما هو الموجود على الملصق؟
نِطَاق
- جميع الأجهزة الطبية وملحقاتها، باستثناء الأجهزة المصممة خصيصًا لمرضى محددين والأجهزة المستخدمة لأغراض البحث والاختبار
- الشركات المصنعة والممثلين المعتمدين
وكالات الإصدار المعترف بها
وكالات الإصدار المعترف بها من قبل UDI هي الكيانات التالية: GS1، و HIBCC، و ICCBBA.
قاعدة بيانات UDI
- يجب على الشركة المصنعة أو ممثلها المعتمد تقديم البيانات المناسبة والحفاظ عليها في قاعدة بيانات UDI.
- يجب فحصها وصيانتها بشكل دوري من قبل الشركة المصنعة
- ستكون بيانات UDI-DI الجديدة متاحة في قاعدة البيانات عند طرح الجهاز في السوق.
- ستكون جميع البيانات المحددة (غير الخاصة) في قاعدة البيانات متاحة للعامة.
- جميع البيانات الموجودة في GHAD وSaudi-DI، مثل اسم الطراز وكود GMDN، دقيقة وصالحة.
لماذا UDI؟
يهدف نظام UDI التابع للهيئة العامة للغذاء والدواء إلى توحيد معايير تحديد الأجهزة الطبية (وملحقاتها). ويسعى نظام UDI إلى زيادة سلامة المرضى وتحسين رعايتهم من خلال تسهيل ما يلي:
زيادة سلامة المرضى
- زيادة سلامة المرضى: في تقارير الأحداث السلبية وغيرها من أنشطة المراقبة بعد التسويق، قم باتخاذ إجراءات تصحيحية للسلامة الميدانية.
- تحسين التعريف والقدرة على التتبع: التحكم في الموانئ وأثناء دورات حياتها، والتعريف، والتوثيق عند نقطة الاستخدام للمريض.
- التعرف على المنتجات المقلدة.
- الاستخدام الآمن والفعال للأجهزة وتقليل الأخطاء الطبية.
- السجلات الصحية الإلكترونية للمريض.
تم استخدامه في جوانب أخرى
- إدارة المشتريات والمخزون
- أنشطة التأمين الطبي
- التحكم في التكاليف ومراقبتها
- استبدال الترميز الداخلي بـ UDI
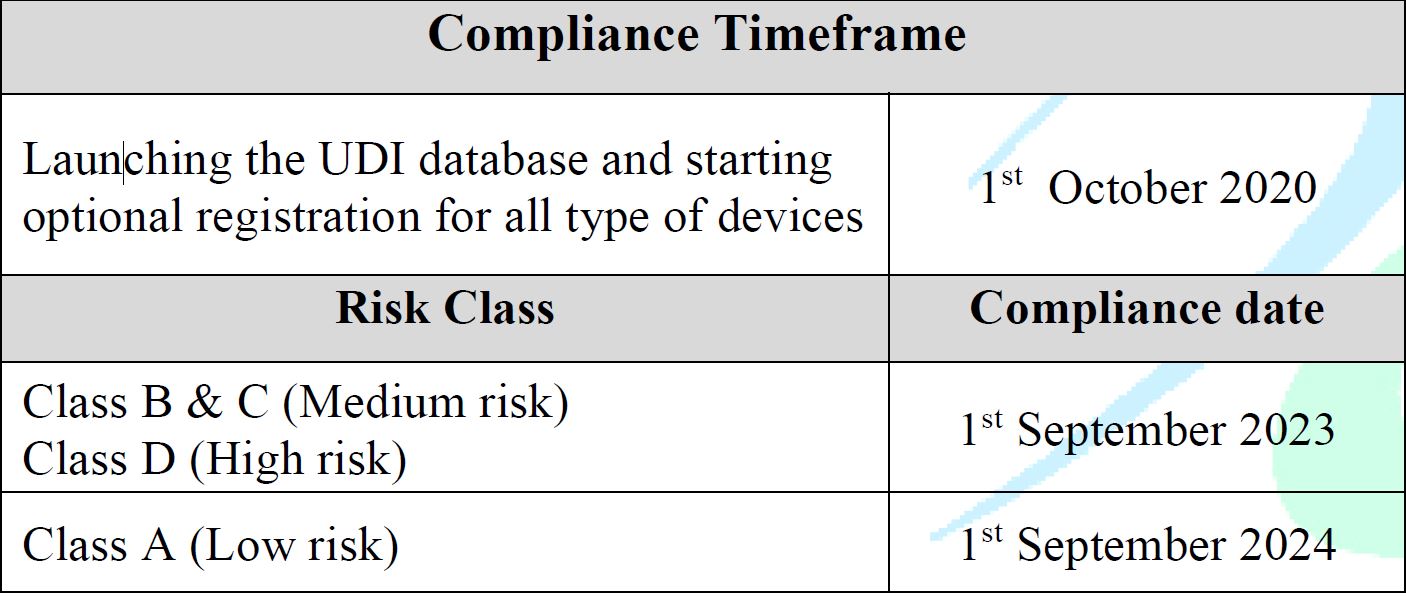
تواريخ سريان الامتثال
- ساري المفعول اعتبارًا من 1 أكتوبر 2020
إطلاق قاعدة بيانات UDI وبدء التسجيل الاختياري لجميع أنواع الأجهزة. - سيتم وضع خطة التنفيذ بناءً على فئة مخاطر المنتج على النحو التالي:
- عالية الخطورة (د): 1 سبتمبر 2023
- المخاطر المتوسطة (ب، ج): 1 سبتمبر 2023
- منخفض المخاطر (الفئة أ): 1 سبتمبر 2024
كيف أقوم بتسجيل منتج جهازي الطبي؟
يمكن للممثلين المعتمدين في المملكة العربية السعودية الوصول إلى هذه المعلومات عبر منصة SFDA UDI. اتصل بنا للحصول على الدعم.
اقرأ المزيد:
عن الكاتب
محرر التنظيمات
نشر من قبل قسم الشؤون التنظيمية في فارمانول للإستشارات، الرياض.
موارد وأدوات
أحداث وفعاليات
الخدمات









